
우리는 물체의 색깔이 어떻게 해서 나타나는지 알아봤다.
Article 1 (Part 1). 빛은 검은색을 흡수하고 흰색은 반사한다
Article 1 ( Part 1). 빛은 검은색을 흡수하고 흰색은 반사한다
흔히들 검은색은 흡수하고 흰색은 반사시킨다고 한다.그런데, 검은색이라서 흡수하고 흰색이라서 반사하는 것이 아니다.주객이 전도된 표현이다.정확한 표현은 빛이 다 흡수가 되면 검은색으
science-scandal.tistory.com
Article 1 (Part 2). 빛은 검은색을 흡수하고 흰색은 반사한다
Article 1 (Part 2). 빛은 검은색을 흡수하고 흰색은 반사한다
Part 1에 이어서 그 원리를 보어의 원자 모델에서 알아보도록 하자 Part 1 1. 빛의 특성 2. 색깔이 나타나는 원리 3. 빛의 흡수 Part 2 4. 보어의 원자 모델 5. 에너지 간격(Bandgap)
science-scandal.tistory.com
그런데, 일반적인 물체들과 금속은 조금 다른것은 광택이 난다.
특히, 금은 노란색이라고 하지 않고 금색이라고 표현할 만큼 색깔을 구분하고 있다. 금 뿐만 아니라 은도 흰색이지만 은색이라고 부르고, 구리도 빨간색이지만 구리색이라고 부른다.
조금더 생각해보면 Article 1 에서 빛의 성분중에 우리가 눈으로 불수 있는 영역은 가시광선영역으로 빨주노초파남보로 구성되어 있다고 했고, 가시광선에서 흡수된 나머지가 반사하면서 색깔을 나타낸다. 근데 가시광선에는 금색, 은색, 구리색도 없으니 어떤색이 흡수되어 금색이나 은색, 구리색을 나타낼수가 없다.
일반적으로 금속은 금속광택으로 노란색이 금색으로 보이고 흰색이 은색으로 빨간색이 구리색으로 보이는 것이다.
그럼 아래 순서대로 알아 보도록 하자
1. 금속은 무엇인가?
2. 금속 결합
3. 금속의 플라즈마 진동(Plasma Frequency)과 광택
4. 금속의 색상
1. 금속은 무엇인가?
학교 다닐때 배운 원소 주기율표를 보면 118종의 원소들 가운데 96종의 원소가 금속으로 분류된다. 자연계에 존재하는 원소 중 산소, 수소, 황, 질소, 그리고 헬륨, 아르곤, 네온과 같은 비활성 기체 원소, 염소, 플루오린과 같은 할로젠 원소 등을 제외한 나머지 대부분은 금속 원소이고 비슷한 성질을 가진 원소들끼리 분류되어 있고 같은 세로줄에 있는 원소들이다.
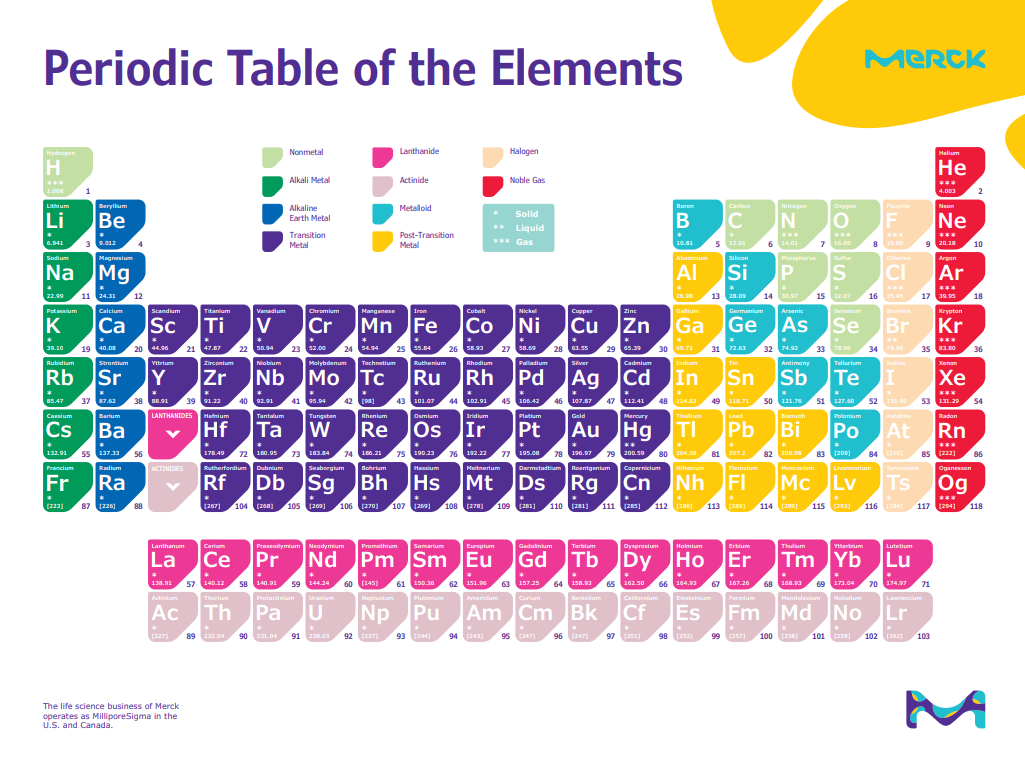
보어의 전자 모델로 다시 이야기 하면, 원소들 중에는 전자를 잃기 쉬운 원소가 있고, 전자를 얻기 쉬운원소도 있고 잃지도 얻지도 않는 원소들도 있다. 그 중 전자를 잃기 쉬운 원소들이 금속이 된다. 이러한 원소들은 금속결합으로, 구리나 철, 금, 은과 같은 원소들이 이에 해당된다
2. 금속 결합
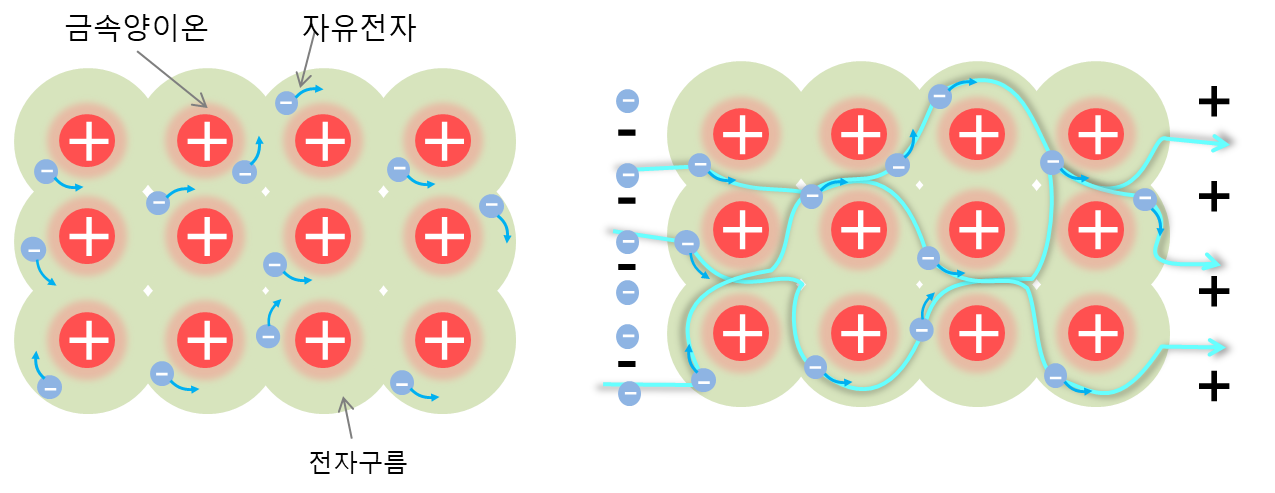
금속 원자는 이온화 에너지가 낮아서 가장 바깥에 있는 전자껍질의 전자와 원자핵이 약하게 결합되어 있어 전자를 쉽게 방출한다. 그중 가장 바깥쪽에 있는 전자는 안쪽의 전자보다 양이온으로 부터 인력이 약하여 전자가 방출되어 금속안을 자유롭게 이동할수 있는 자유 전자가 되고, 전자를 잃은 금속 원자는 양이온를 띄게된다.
양이온을 띤 금속 원자는 반발력에 의해 서로 떨어져야 하지만 가장 바깥쪽 전자껍질이 서로 겹쳐 있고, 음이온의 자유전자가 자유롭게 이동하기 때문에 정전기적 인력으로 인해 서로 떨어지지 않고 결합된 상태로 있을수 있다. 이러한 원리로 금속이 고체일때 원자들이 규직적인 배열로 강하게 결합하여 단단한 성질을 갇게 된다.
따라서, 양이온를 띤 금속 원자들 사이를 자유 전자가 원자들 사이를 자유롭게 이동하는 전자들에 둘러 쌓여, 즉 전전자바다에 의해 양이온를 띤 금속 원자핵은 정전기적 인력에 의한 결합을 유지한다. 이런 결합을 금속 결합이라고 한다. 이러한 전자바다는 금속을 망치로 내리쳐도 전자가 다른 원자에 있는 전자를 채워 넣는 형태로 움직여서 깨어지지 않고 결합을 유지 하고 있는 것이다.
3. 금속의 플라즈마 진동(Plasma Frequency) 과 광택
금속안의 자유전자들의 진동하는것을 플라즈몬(Plasmon)이라고 하며 이러한 플라즈몬은 금속의 광학적 성질을 변화시킨다. 금속 표면에 닿은 빛의 진동수가 플라즈마 진동수(Plasma frequency)보다 작은(느린)경우에는 자유전자는 빛의 진동수에 따라 진동을 한다. 이때 빛의 에너지는 자유전자의 진동에 사용되지만, 자유전자는 원래의 빛과 같은 진동수의 빛을 재 방출한다.
그리고 빛의 진동수가 플라즈마 진동수 보다 높은(빠른) 경우 자유전자가 움직일수 있는 속도의 한계를 넘게 되면서 금속 표면의 자유전자가 움직이지 않아 그대로 금속안으로 들어가면서 그 빛은 투과하게 된다.

대부분의 금속의 플라즈마 진동수는 자외선 대역이기 때문에, 진동수가 낮은 가시광선은 자유전자에 의해 차단되어 금속으로 들어갈수 없으며 자유전자에 의해 같은 진동수의 가시광선으로 금속 밖으로 튕겨져서 마치 반사되는 것처럼 되면서 거울과 같이 반짝거리는 특성으로 광택이 나타나게 된다. 같은 진동수를 반사시킨다는 것은 같은 색의 빛을 낸다는 의미이다.그리고 특정 진동수 대역의 빛은 에너지 대에 흡수되면서 나머지 가시광선이 반사되어 금속의 색상을 결정하게된다.

4. 금속의 색상
금속은 금속마다 광택의 색이 다르다. 금은 노란색에 광택을 내고, 은은 하얀색에 광택이 내고 구리는 붉은색에 광택을 나타낸다.
금속도 동일한 이유로 금은 푸른색을 흡수하고 적색과 녹색을 반사해서 황금색으로 나오고, 구리는 적색을 잘 반사하고, 청색과 녹색의 빛도 반사하기 때문에 백색을 띤 적색으로 보인다. 철은 가시광선 전역을 반사하여 회색을 띤 금속 광택을 나타낸다
그럼 흡수의 색을 결정하는 것은 자유전자의 진동수와 에너지 준위에 따라 달라진다. 에너지 준위는 원자의 기본구조에서 궤도마다 전자가 갖는 에너지 값이 정해져 있다. 물질마다 갖고 있는 이런 에너지 값을 에너지 준위라고 한다.
전자는 에너지를 흡수하면 높은 궤도로, 에너지를 방출하면 낮은 궤도로 이동한다, 전자가 얼마나 높은 궤도에서 낮은 궤도로 이동하는지에 따라 방출하는 빛의 종류와 색이 다르다.
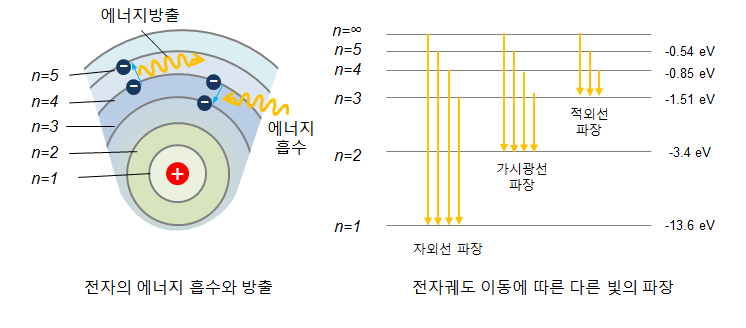
금은 가시광선 중 노란색 계열의 진동수보다 자유전자의 진동수가 빨라서 동일한 진동수로 자유전자를 방출하고 가시광선 중 초록색에서 보라색계열은 금이 가진 자유전자의 진동수가 느려서 동일한 진동수로 방출하지 못하고 흡수하게 된다. 그래서 금은 노란색의 광택을 낸다.
은(Ag)은 자유전자의 진동수가 금보다 빨라서 모든 가시광선을 흡수하고 동일한 진동수로 재방출 하면서 흰색에 광택을 나타낸다. 또한 은(Ag) 은 자유전자의 밀도가 높고 자유전자의 진동수가 빨라서 반사율이 높다. 구리는 금보다 자유전자의 진동수가 느려서 초록색계열이 흡수되면서 붉은색의 광택을 나타내게 된다.
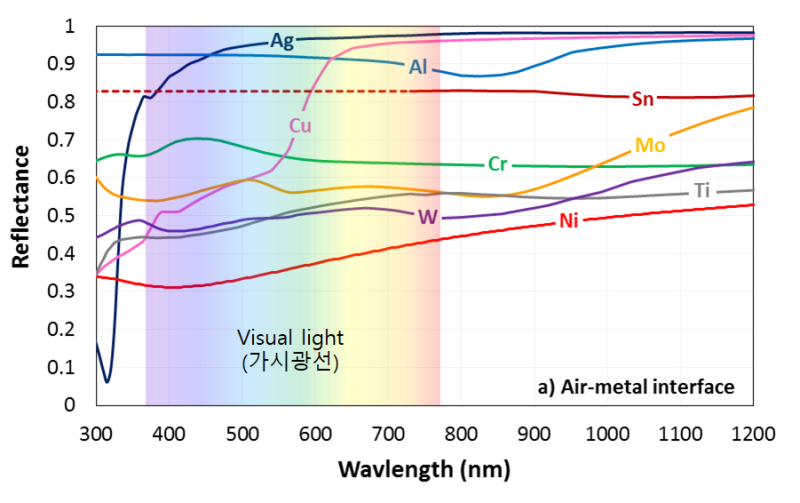
결론적으로 금속의 광택은 자유전자에 의해서 가시광선이 흡수되면 동일한 진동수로 재 방출하면서 광택이 나고 금속마다 자유전자의 진동수가 달라서 방출하는 빛이 달라서 색깔이 다르게 나타나는 것이다.
'Science Article' 카테고리의 다른 글
| Article 12. 인공지능의 역사 (16) | 2024.04.25 |
|---|---|
| Article 11. 하늘은 파란색인데 노을은 왜 붉은색일까? (10) | 2024.04.25 |
| Article 9. 겨울철 패딩이나 털옷은 왜 따뜻할까 (22) | 2024.04.25 |
| Article 8. 도로가 어떻게 반사가 될까? (16) | 2024.04.24 |
| Article 7. 달리는 기차에서 떨어진 공은 왜 뒤로 가지 않는걸까? (22) | 2024.04.24 |



